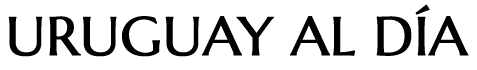马德里,14(欧洲出版社)
美国洛克菲勒大学的科学家研发的新型CD40激动剂免疫刺激抗体2141-V11,在参与1期临床试验的12名患者中,成功使6名患者的转移性肿瘤缩小,其中2名患者的肿瘤完全消失。
这项发表在《癌细胞》(Cancer Cell)杂志上的研究旨在证明一种改良型CD40激动剂抗体对癌症患者的疗效。这些抗体最初在动物模型中展现出巨大的潜力,但在人类身上效果有限,且伴有显著的不良反应。
2018 年,洛克菲勒大学 Jeffrey V. Ravetch 实验室使用转基因小鼠进行的初步实验表明,他们设计的新型药物更加有效,在产生抗肿瘤免疫反应方面的效力提高了 10 倍。
他们随后改变了给药方式,不再采用传统的静脉注射。由于CD40受体分布广泛,太多非癌细胞吸收了该药物,从而产生了毒副作用。取而代之的是,他们将药物直接注射到肿瘤内。“当我们这样做时,我们只观察到轻微的毒性,”Jeffrey V. Ravetch指出。
充满希望的结果
如今,这项小规模人体试验已显示出未来临床应用的良好前景。该研究纳入了12名患有不同类型转移性癌症的患者,具体包括黑色素瘤、肾细胞癌和不同类型的乳腺癌。
两名完全缓解的患者分别患有黑色素瘤和乳腺癌,这两种癌症都具有侵袭性和复发性。
“那位黑色素瘤患者的腿部和足部有数十个转移性肿瘤,我们只在她大腿的一个肿瘤里注射了药物,”拉维奇解释说。“对这个肿瘤注射多次后,其他肿瘤都消失了。转移性乳腺癌患者也出现了同样的情况,她的皮肤、肝脏和肺部都有肿瘤。尽管我们只在她的皮肤上注射了药物,但所有肿瘤都消失了,”她解释说。
2141-V11 创新能够以优化的方式与抗体 Fc 片段的抑制受体 FcyRIIB 结合,其直接肿瘤内给药可以降低以前形式观察到的全身毒性,此外还可以增强树突状细胞和 T 淋巴细胞的局部活化,正如 CNIO-HMarBCN 癌症免疫治疗临床研究部门负责人 Luis Álvarez Vallina 在向 SMC Spain 发表的声明中所解释的那样。
“该策略可应用于不同类型的肿瘤,尤其是那些易于局部注射的肿瘤(皮肤、淋巴结、膀胱、乳腺),”Álvarez 强调道。然而,他也强调,需要对该药物进行更长期的随访,以确认疗效的持久性,并确定能够更好地筛选患者的生物标志物。
刺激免疫活动
第一作者、Ravetch 实验室客座助理教授兼纪念斯隆凯特琳癌症中心肿瘤内科医生 Juan Osorio 博士说,肿瘤组织样本显示出药物刺激的免疫活动,包括不同类型的树突状细胞、成熟 T 细胞和形成淋巴结样聚集体的 B 细胞。
“这种药物在肿瘤内创造了一个免疫微环境,并用这些三级淋巴结构将其取代,”奥索里奥强调道,并指出这与更好的预后和对免疫疗法的反应有关。此外,当免疫系统识别癌细胞时,这些三级淋巴结构会迁移到未注射的肿瘤区域。
基于这些发现,Ravetch 实验室已启动多项临床试验,并与纪念斯隆凯特琳癌症中心和杜克大学的研究人员合作。这些 1 期和 2 期试验旨在探究 2141-V11 对特定癌症(例如膀胱癌、前列腺癌和胶质母细胞瘤)的效果,共有近 200 名参与者参与。
他们希望借此弄清药物在某些患者身上有效,而在其他患者身上无效的原因,从而找到改变这一现状的方法。例如,临床试验中癌症消失的两名患者在研究开始时就具有较高的T细胞克隆性,这可能是该药物有效的必要条件之一。