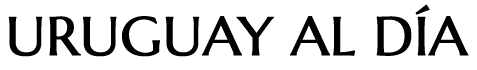МАДРИД, 14 (EUROPA PRESS)
Новая версия иммуностимулирующего антитела-агониста CD40, названная 2141-V11 и разработанная учеными Рокфеллеровского университета (США), успешно уменьшила метастатические опухоли у шести из 12 пациентов, участвовавших в исследовании фазы 1; у двух из них опухоль полностью исчезла.
Исследование, опубликованное в журнале Cancer Cell, было призвано продемонстрировать эффективность усовершенствованной формы антител-агонистов CD40 у онкологических пациентов. Эти антитела первоначально продемонстрировали высокий потенциал в животных моделях, но имели ограниченное воздействие на людей и вызывали значительные побочные эффекты.
В ходе первоначального эксперимента, проведенного в 2018 году с использованием генетически модифицированных мышей, лаборатория Джеффри В. Раветча в Рокфеллеровском университете показала, что новая форма разработанного ими препарата оказалась более эффективной и обладала в 10 раз большей силой в формировании противоопухолевого иммунного ответа.
Затем они изменили способ введения препарата, который традиционно вводился внутривенно. Поскольку рецепторы CD40 широко распространены, препарат поглощался слишком большим количеством нераковых клеток, что вызывало токсические побочные эффекты. Вместо этого они вводили препарат непосредственно в опухоли, интратуморально. «При этом мы наблюдали лишь лёгкую токсичность», — отметил Джеффри В. Раветч.
ОБНАДЕЖНЫЕ РЕЗУЛЬТАТЫ
Небольшое исследование на людях показало многообещающие результаты для будущего клинического применения. В исследовании приняли участие 12 пациентов с различными типами метастатического рака, в частности, меланомой, почечно-клеточным раком и различными типами рака молочной железы.
У двух пациентов, у которых наступила полная ремиссия, была меланома и рак молочной железы соответственно, оба заболевания были известны своей агрессивностью и рецидивирующим течением.
«У пациентки с меланомой были десятки метастатических опухолей в ноге и стопе, а мы ввели препарат только в одну опухоль на бедре», — пояснила Раветч. «После нескольких инъекций в эту опухоль все остальные исчезли. То же самое произошло и с пациенткой с метастатическим раком молочной железы, у которой также были опухоли в коже, печени и лёгких. И хотя мы ввели препарат только в кожу, мы увидели, что все опухоли исчезли», — пояснила она.
Инновация 2141-V11 обладает способностью связываться оптимизированным образом с ингибиторным рецептором Fc-фрагмента антитела, называемого FcyRIIB, а ее прямое внутриопухолевое введение позволяет снизить системную токсичность, наблюдавшуюся при использовании предыдущих форматов, а также усилить локальную активацию дендритных клеток и Т-лимфоцитов, как объяснил руководитель отдела клинических исследований в области иммунотерапии рака в CNIO-HMarBCN Луис Альварес Валлина в своих заявлениях для SMC Spain.
«Эту стратегию можно применять к различным типам опухолей, особенно к тем, которые доступны для местных инъекций (кожа, лимфатические узлы, мочевой пузырь, молочная железа)», — подчеркнул Альварес. Однако он подчеркнул, что необходимо более длительное наблюдение за препаратом для подтверждения стойкости ответа и определения биомаркеров, которые позволят более эффективно отбирать пациентов.
СТИМУЛИРОВАННАЯ ИММУННАЯ АКТИВНОСТЬ
«Образцы тканей опухолей выявили стимулированную лекарствами иммунную активность, включая различные типы дендритных клеток, зрелых Т-клеток и В-клеток, которые формировали агрегаты, похожие на лимфатические узлы», — рассказал первый автор Хуан Осорио, доктор философии, приглашенный доцент в лаборатории Раветча и врач-онколог в Мемориальном онкологическом центре имени Слоуна-Кеттеринга.
«Препарат создаёт иммунное микроокружение внутри опухоли и фактически заменяет его этими третичными лимфоидными структурами», — подчеркнул Осорио, уточнив, что это связано с улучшением прогноза и ответа на иммунотерапию. Более того, эти третичные лимфоидные структуры мигрируют в неинъецированные участки опухоли, когда иммунная система распознаёт раковые клетки.
На основании этих результатов было инициировано несколько дополнительных клинических испытаний, в которых лаборатория Равеча сотрудничает с исследователями из Мемориального центра имени Слоуна-Кеттеринга и Университета Дьюка. В этих исследованиях первой и второй фазы изучается влияние 2141-V11 на конкретные виды рака, такие как рак мочевого пузыря, рак предстательной железы и глиобластома. В них приняли участие почти 200 человек.
Таким образом, они пытаются выяснить, почему препарат действует у одних пациентов и не действует у других, чтобы найти способы изменить это. Например, у двух пациентов, участвовавших в клиническом исследовании, у которых рак исчез, в начале исследования наблюдалась высокая клональность Т-клеток, что может быть одним из условий эффективности препарата.